Laboratorium
„Wiedza jest drugim słońcem dla tych, którzy ją posiadają…” – Heraklit z Efezu
Czy wiesz, że…
- Ciało c
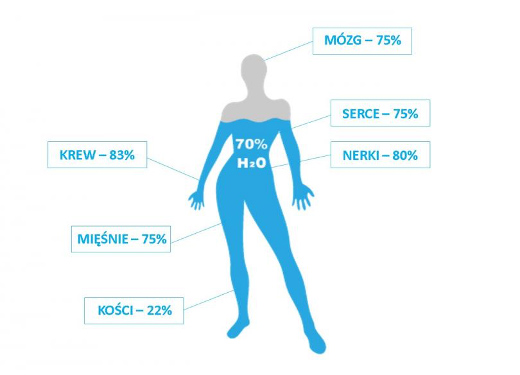 złowieka, w zależności od wieku, składa się w 45 % (wiek podeszły), do około 65 %- 70 % ( ludzie dorośli), a nawet 78 % (dzieci do 2 roku życia) z wody. Woda jest składnikiem wszystkich tkanek i płynów ustrojowych, koniecznym do pełnienia ich funkcji fizjologicznych, a więc życiowych.
złowieka, w zależności od wieku, składa się w 45 % (wiek podeszły), do około 65 %- 70 % ( ludzie dorośli), a nawet 78 % (dzieci do 2 roku życia) z wody. Woda jest składnikiem wszystkich tkanek i płynów ustrojowych, koniecznym do pełnienia ich funkcji fizjologicznych, a więc życiowych. - Twardość wody jest skutkiem obecności szeregu różnych rozpuszczonych w niej jonów metali wielowartościowych, kationów magnezu i wapnia, dlatego też zwykle wyraża się ją w miligramach węglanu wapnia na litr. ( CaCO3 / l ).
Twardość to tradycyjna miara zdolności wody reagowania z mydłem. Woda twarda do wytworzenia piany wymaga zauważalnie więcej mydła, niż woda miękka.W zależności od tego jakie związki bierzemy pod uwagę określając twardość, rozróżniamy:- twardość węglanową – zawartość węglanu wapnia oraz węglanu magnezu, sole te wytracają się w postaci tzw. kamienia, na przykład po zagotowaniu wody,
- twardość niewęglanową – zawartość w wodzie innych soli wapnia , magnezu oraz innych minerałów np. siarczanów miedzi, siarczanów magnezu, chlorków wapnia czy chlorków magnezu,
- twardość ogólną ( całkowitą ) – suma zawartości węglanów i innych soli mineralnych.
| Stopień twardości wody | [mg CaCO3] | [stopnie niemieckie] |
|---|---|---|
| Woda bardzo miękka | < 100 | < 5,6 |
| Woda miękka | 100-200 | C5,6-11,2 |
| Woda średnio-twarda | 200-350 | 11,2-19,6 |
| Woda twarda | 350-550 | 19,6-30,8 |
| Woda bardzo twarda | > 550 | > 30,8 |
 Jaka woda i dla kogo…
Jaka woda i dla kogo…
- Wody z dominującym udziałem chlorków i sodu są odpowiednie do picia przy intensywnym wysiłku fizycznym, w czasie uprawiania sportu oraz w wysokich temperaturach otoczenia.
- Wody z niską zawartością sodu i chlorków (<20 mg / l ) są odpowiednie dla osób, którym zalecono ograniczenie tych składników w diecie oraz dla małych dzieci i niemowląt.
- Wody z dominującym udziałem magnezu są odpowiednie do picia dla osób poddanych stresowi. Magnez bowiem to biopierwiastek bez którego prawidłowe funkcjonowanie naszego układu nerwowego i mózgu nie byłoby możliwe, a który jest podczas stresujących sytuacji szybko zużywany przez organizm. Warto wiedzieć, że podczas 10 minutowego silnego zdenerwowania, nasz organizm zużywa tyle magnezu, ile przeciętnie wynosi dzienne zapotrzebowanie na ten pierwiastek. Magnez stabilizuje funkcje układu nerwowego i usprawnia jego pracę. Magnez pomaga również regulować poziom wapnia i poprawia wchłanianie potasu. Rozszerza tętnice i chroni przed zawałem. Wpływa na utrzymanie prawidłowego rytmu serca, dlatego osoby pijące wodę, która zawiera dużą ilość magnezu, rzadziej zapadają na choroby serca.
Wody uznane jako naturalne wody mineralne:
Pobierz Obwieszczenie (PDF)
A co z jakością wody?
Bardzo duże znaczenie dla jakości wody ma występowanie w niej różnego rodzaju jonów i tak…
Żelazo – już kilka mg / l czyni wodę nieprzydatną w przemyślę spożywczym,
Amoniak ( jon amonu) – jest końcowym produktem rozkładu białka, dlatego nawet niewielkie jego ilości > 0,5 mg / l dyskwalifikują wodę z higienicznego punktu widzenia,
Azotyny – ich obecność w wodzie świadczy o nie ukończonym procesie biologicznego samooczyszczenia wody (nitryfikacji), co dyskwalifikuje wodę, podobnie jak wodę zawierającą jon amonu,
Azotany – ich obecność, nawet w ilości 50 – 100 mg / l przy braku azotynów i jonu amonowego jest nieszkodliwa, chociaż ujemnie świadczy o pochodzeniu wody, dlatego wody zawierające azotany wymagają ścisłej kontroli mikrobiologicznej,
Chlorki – jako chlorek sodu nie stanowią groźnego zanieczyszczenia, jednak w niektórych przemysłach, np. w browarnictwie woda nie powinna zawierać nadmiernej ilości ich jonów,
Siarkowodór – występuje rzadko w wodach i jest łatwo wykrywalny na podstawie zapachu,
Wapń – w przemyśle owocowo – warzywnym woda stosowana do produkcji soków powinna zwierać małe ilości tego pierwiastka, z kolei do wyrobów konserw warzywnych (groszek, fasolka) powinna zawierać większe ilości, powoduje to minimalne utwardzenie skórki warzyw i ogranicza przechodzenie skrobi do zalewy.
Miłej lektury 😉


